| Autor |
Nachricht |
|
bdomanig
|
Betreff des Beitrags: Frage zu Prüfungsfragen  Verfasst: Verfasst: 26.02.2011, 14:02 |
|
| Versuchskaninchen |
 |
 |
Registriert: 06.09.2010, 16:24
Beiträge: 83
|
|
Hallo zusammen!
Hoffentlich kann mir jemand von euch die Antwort auf folgende Frage geben:
Wie kann man mit der Nernst'schen Gleichung vorraussagen ob eine Reaktion freiwillig ablaufen wird?
Ich hab sowohl im 2010 als auch in den 2009 Skripten nachgeschaut und auch im Mortimer, jedoch leider nichts gefunden.
Die Nernst Gleichung ist doch:
E = E° + ((2,303*R*T)/nF) * log (a(ox)/a(red))
oder?
Aber wie seh ich dann ob die Reaktion freiwillig abläuft?
lg b
_________________ Masterstudent Biotech // Vice-President Club Biotech // Referent für Bildung und Politik der ÖH BOKU
___________________________________________________________________________________________
„Wer sich Steine zurechtlegen kann, über die er stolpert, hat Erfolg in den Naturwissenschaften.“ Zitat von
|
|
  |
|
 |
|
Luci
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 27.02.2011, 01:57 |
|
| Moderator |
 |
 |
Registriert: 16.12.2006, 18:34
Beiträge: 764
Wohnort: 1180 Wien
|
Stichwort: endotherm und exotherm 
|
|
  |
|
 |
|
bdomanig
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 02.03.2011, 06:33 |
|
| Versuchskaninchen |
 |
 |
Registriert: 06.09.2010, 16:24
Beiträge: 83
|
Luci hat geschrieben: Stichwort: endotherm und exotherm  ja danke für die antwort  ) so einfach und doch so schwer  vielen dank _________________ Masterstudent Biotech // Vice-President Club Biotech // Referent für Bildung und Politik der ÖH BOKU
___________________________________________________________________________________________
„Wer sich Steine zurechtlegen kann, über die er stolpert, hat Erfolg in den Naturwissenschaften.“ Zitat von
|
|
  |
|
 |
|
Cherryfruit
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 02.03.2011, 18:22 |
|
| Versuchskaninchen |
 |
 |
Registriert: 03.03.2010, 19:09
Beiträge: 48
|
|
Hey!
Bei der Prüfung gab es mal folgende Frage zum Siedediagramm, die ich leider nicht ganz verstehe, also beantworten kann.
Wäre super wenn mir die wer erklären könnte bzw. mir sagen könnte ob ich mit meinen behauptungen richtig liege
a) Wie hei?n die beiden Kurven in folgendem Sidediagramm (direkt in die Graphik einzeichnen)? --> okay das weiß ich noch!
b) Wie hoch ist die Siedetemperatur der reinen Substanz A?
c)Wie hoch ist die Siedetemperatur der reinen Substanz B?
--> kann ich wahrscheinlich aus dem Diagramm ablesen(?)
d) Sie haben eine Mischung mit der Zusammensetzung: Molanteil von A = 0.2. Ab welcher Temperatur beginnt die Mischung zu sieden?
e) Welche Zusammensetzung (Molanteil von A) hat die Gasphase, wenn diese Mischung siedet?
f) Welche Zusammensetzung (Molanteil von A) hat die Mischung bei 70°C in der Gasphase und der fl?gen Phase?
g) Wieviele Trennstufen ben?en sie mindestens, um eine Mischung zu erhalten, die weniger als 20% (Mol%) B enth?? -einzeichnen!
Bei d) - g) hab ich leider keine Ahnung!
Bitte um Hilfe!
MFG
|
|
  |
|
 |
|
Luci
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 02.03.2011, 22:30 |
|
| Moderator |
 |
 |
Registriert: 16.12.2006, 18:34
Beiträge: 764
Wohnort: 1180 Wien
|
|
du kannst alles aus dem Diagramm ablesen!
Wenn du verstehst was die Kurven aussagen. d.h in welchem Bereich ist der flüssige und in in welchem Bereich ist der gasförmige Zustand! -->
wenn du das weißt, dann musst du dir auf der x Achse den Anteil von 0,2 anschauen, eine Gerade nach oben ziehen und bei der Temperatur wo der Schnittpunkt mit der jeweiligen Kurve ist, ist auch z.b die Siedetemperatur
und alle anderen Punkte kannst du dir auch auf diese Art und Weise ablesen
zum Thema Trennstufen - sollte im Skript zu finden sein. Das ist ebenfalls graphisch zu lösen. Im ESI und MTV Skript ist es auch drinnen
kleine Hilfe mit der angefügten Graphik
| Dateianhänge: |
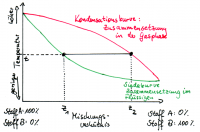
siedediagramm.png [ 120.96 KiB | 484-mal betrachtet ]
|
|
|
  |
|
 |
|
Cherryfruit
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 03.03.2011, 20:47 |
|
| Versuchskaninchen |
 |
 |
Registriert: 03.03.2010, 19:09
Beiträge: 48
|
|
Wow Danke Luci! Die Skizze ist echt hilfreich!
Hätte da noch eine kleine Fragen, und zwar:
a)Zeichnen Sie die Titrationskurve von 10 ml NaOH (c = 0,1mol/L), die tropfenweise mit HCl (c = 0,1 mol/L) titriert wird.
Bestimmen Sie Anfangspunkt, Äquivalenzpunkt, Endpunkt der Titration (auch Berechnungen!). Welche(n) Indikator(en)
würden Sie verwenden? (Ankreuzen)
Mir ist bei der Frage eigentlich eh alles klar, aber was wird gemeint mit "auch Berechnungen"???
Kann mich nicht an eine Berechnung erinnern?
MFG
|
|
  |
|
 |
|
Luci
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 04.03.2011, 17:49 |
|
| Moderator |
 |
 |
Registriert: 16.12.2006, 18:34
Beiträge: 764
Wohnort: 1180 Wien
|
Zitat: Bestimmen Sie Anfangspunkt, Äquivalenzpunkt, Endpunkt der Titration naja mit Berechnung ist auch Berechnung gemeint  Wie du bei welchen Punkt auf die Konzentration kommst, mit c=?!?! Stichwort: Stoffmenge und Volume Dann pOH = ...... was ist pH?.... und dann willst du die Konzentration der H+ Ionen schaus dir im Mortimer an, da ist eine Tabelle die bereits ausgefüllt ist. Versuch mal jeden einzelnen Schritt zu rechnen! und so sollte es auch bei der Prüfung sein lg Luci
|
|
  |
|
 |
|
Mobi
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 16.04.2011, 13:32 |
|
| Versuchskaninchen |
 |
 |
Registriert: 04.12.2010, 18:54
Beiträge: 50
|
|
hab da auch eine frage:
es gibt eine Prüfungsfrage wo es um den [Cu(NH3)4] 2+ komplex geht und da steht dass man die form zeichen soll und den Komplex erklären soll
Da is aber nicht die Strukturformel gemeint oder?
und wie erklär ich den komplex?
lg:)
|
|
  |
|
 |
|
Naiya
|
Betreff des Beitrags: Re: Frage zu Prüfungsfragen  Verfasst: Verfasst: 18.04.2011, 13:10 |
|
| Zellenzähler/in |
 |
 |
Registriert: 06.11.2006, 18:09
Beiträge: 309
Wohnort: Wien
|
Naja, wie willst du einen Komplex sonst zeichnen?  Ich würde mal stark zur Struktur raten. Im Bezug aufs "Erklären" würde ich mal sagen - am besten nach dem Lewis-Konzept! Was reagiert womit - welcher Teil des Komplexes fungiert somit als Base und welcher als Säure? So würde ich es versuchen...
|
|
  |
|
 |
|






